いろいろな塩の違いとは?
home >>> いろいろな「塩」の違いとは? TOP >>> 具体的な塩の違い >>> 【参考】釜焚結晶と天日結晶
【参考】釜焚結晶と天日結晶
それは温度と時間の違いから起こること
このページでは「釜焚結晶」と「天日結晶」の違いに焦点を絞ります。それはまず海水を濃縮する温度にあります。また高温と低温では、濃縮される(水分が蒸発する)速度も違うので、時間の違いという面もあります。
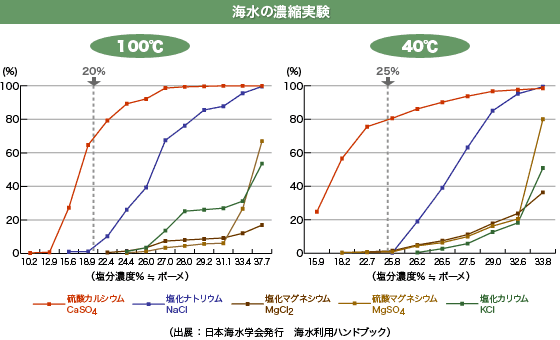
下のグラフは、海水を40℃と100℃で濃縮したとき、海水の各成分がどんなふうに固まっていくか(塩になっていくか)を示したグラフです。以下、「○○成分が固まる」は「析出する」とします。
釜で焚く場合は、沸騰するぐらいとして、およそ100℃。左側のグラフです。一方、例えばベトナム・カンホアの場合、塩を作る乾期の日中の最高温度は40℃を超え、最低でも30℃前後。よって、ほぼ右側の40℃のグラフが天日と思ってください。
両方とも、横軸(X軸)は海水の塩分濃度。グラフは析出が始まるところから始まり、右へいくほど時間とともに濃くなっていきます。そして縦軸(Y軸)は各成分がその塩分濃度で何%析出したかを示しています。例えば硫酸カルシウムは海水中に約4%含まれていますが、そのうち半分の2%が析出したとすると、グラフ(縦軸)は50%を示します。
線が平らなほどゆっくり析出していて、線が急なほど一気に析出しています。この実験は、海水の成分で比較的多い上位5種類のデータです。詳しくは、「海水について」をご覧ください。では、2つのグラフを比べてみましょう。
まずは全体的に見てみる
どちらも大まかには似てますが、5つの成分ともに、右の40℃の方が線が滑らかです。40℃の方は、青色のNaClを中心軸にして、上のカルシウム分と下のマグネシウム分・カリウム分が対照的なカーブを描きながら、ジワジワと析出していることが分かります。また、グラフの横軸は塩分濃度です。時間にすると、40℃(天日)のグラフは1〜2週間ほどの出来事で、100℃(釜焚き)の方は一昼夜ほどの出来事です。X軸を時間にすると、40℃の方はほとんど線が平らなぐらい、ゆっくりと塩が析出していることになります。
次に、各成分ごとに見てみる
■カルシウム分(硫酸カルシウム)
味は淡いエグ味。性質は、この5つの成分のうち、最も溶けにくい。ですから、塩作りでは(海水を濃縮すると)一番最初に析出します。40℃に比べ、100℃ではグラフの線が急になっています。
この硫酸カルシウムは風変わりな物質です。0℃から40℃ぐらいまでは、他の多くの物質のように温度が高くなるにつれ、より溶けやすくなりますが、40℃ぐらいを境に反対にどんどん溶けにくくなり、100℃では最も溶けにくくなります。(100℃では0℃より溶けにくくなります) つまり、40℃が最も溶けやすい温度で、100℃が最も溶けにくい温度です。したがって、40℃と100℃での析出の様子を比べると、100℃では一気に析出し、グラフの線が急になるのです。一気に析出すると、他の成分は混じりにくいため、硫酸カルシウムだけでコチコチに(硬く)なります。それに比べ、ジンワリと固まりになる40℃の方では、カルシウム分は他の成分とも混ざってサクサクと緩く固まるため、塩として溶かす際は、比較的溶けやすくなります。
塩辛味の成分。線の滑らかさは若干違えど、だいたい同じ。顕著に違う点は析出のスタートの濃度です。100℃では20%ぐらい、そして40℃では25%ぐらいです。「釜焚結晶」では、通常濃度20%ぐらいになった『濃い海水』を釜に入れて焚き始めます。そして、一般の「天日結晶」では(カンホアの塩は違いますが)、25%ぐらいになった『濃い海水』を塩を析出させる塩田(結晶池)に入れて結晶させ始めます。それらを裏付ける違いです。=> 【参考】天日製法とは?
■マグネシウム分(塩化マグネシウム・硫酸マグネシウム)
■カリウム分(塩化カリウム)
マグネシウム分は苦味、カリウム分は酸味の成分。100℃に比べ、40℃の方が、3つとも揃って似たようなカーブを描きながら析出しいています。海水の苦味(マグネシウム分)と酸味(カリウム分)のバランスを保ちながら塩が出来ていくのが分かります。
■カリウム分(塩化カリウム)
「各成分の味と性質」で、カリウム分(塩化カリウム)は、ナトリウム分(塩化ナトリウム)よりも、水に溶けやすいと説明しました。ただしそれはそれぞれ単体で水に溶かした場合で、実はその差は僅かです。しかし「海水について」にもあるとおり、海水に含まれる塩化カリウムは2.1%、塩化ナトリウムは77.9%ですから、塩化ナトリウムの方が圧倒的に多い(濃い)という違いがあります。そのため、海水を濃縮すると、圧倒的に多い塩化ナトリウムの方が早くに析出し始め、少ない塩化カリウムはそのしばらく後から析出を始めます。
最後にもっと単純に見てみる
こうしてデータで見ていくと、難しく感じるかも知れませんが、想像してみてください。天日で塩が出来始めてから1〜2週間かけて塩になっていく様子と、釜で焚いて一昼夜で塩になっていく様子を。より低温で長い時間の方が、より規則的に5つの成分が塩が析出していきます。
次のページの前に
次のページは天日製法の具体的解説です。
ベトナムの一般の天日製法とカンホアの塩の天日製法、2つ実例を挙げながら、「天日製法とは実際にはどうしているのか?」・・・海水をただ単純に天日に干しているだけではありません。先人たちの知恵がうかがえます。そして、「天日製法」だからといって、決まった成分・味の食塩にならないこと。また、完成するまでの隅々の工程の違いによっていろんな成分・味の塩になることが分かります。